安徽省宣城市2025届九年级学情调研物理试卷答案试卷答案,炎德英才答案网站目前收集并整理关于安徽省宣城市2025届九年级学情调研物理试卷答案试卷答案得系列试题及其答案,更多试题答案请关注我们
安徽省宣城市2025届九年级学情调研物理试卷答案试卷答案
以下是该试卷的部分内容或者是答案亦或者啥也没有,更多试题答案请关注微信公众号:趣找答案/直接访问www.qzda.com(趣找答案)

10.B【考查点】本题考查有机化合物
【解析】甲醇属于醇类,可以发生取代反应,甲醇分子中不含不饱和碳原子,不能发生加成反应,A错误;乙酸分子中含有一C00H,可与饱和碳酸氢钠溶液反应生成C02,乙醇与饱和碳酸氢钠溶液不反应,故可用饱和碳酸氢钠溶液鉴别二者,B正确;烷烃的沸点随着碳原子数的增加而升高,而碳原子个数相同时,支链越多,沸点越低,C错误;戊二烯的分子式为C,H,[点拨]链状烷烃同分异构体沸点规律
环戊烷()的分子式为CH
,二者分子式不同,不互为同分异构体,D错误
11.D【考查点】本题考查物质结构与元素周期律
【解析】由短周期主族元素“Z的最外层电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍”可知,W和X的最外层电子数之和为偶数,且小于8,结合“W、X、Y、乙为原子序数依次增大的短周期主族元素”“W和X的单质常温下均为气体”可知,W为氢元素、X为氨元素;故Z的最外层电子数为6,Y的最外层电子数为3,结合原子序数:Z>Y>X(N)可知,Z为硫元素、Y为铝元素
同周期元素从左至右,原子半径逐渐减小,则原子半径:A>S,结合第三周期元素原子半径大于第二周期元素原子半径(除Li外)、H在周期表中原子半径最小可知,原子半径:AI>S>N>H,A错误;H与N能形成NH,、N2H等多种化合物,B错误;A1,O,属于两性氧化物,可与强碱发生反应生成盐和水,C错误;(NH)2S为离子化合物,既含离子键又含共价键,D正确
12.B【考查点】本题考查水溶液中的离子平衡
【解析】当-lgc(Ba2)=5.1,即c(Ba2+)=1×l05.1mol·L时,溶液中阴离子浓度:d<c,c、d两点均在沉淀溶解平衡曲线上,则溶度积常数Kp:d<c,结合“相同温度下,K,(BaS0,)<K,(BaCO,)”可知,曲线①、②分别代表BaS04、BaC0,的沉淀溶解平衡曲线,A错误;曲线①上存在坐标(6.0,4.0),即-lgc(Ba2+)=6.0,-lgc(S0)=4.0,有c(Ba2*)=1×106mol·L,c(S0)=1×104mol·L,则该温度下K,(BaS04)=c(Ba2)·c(S0?)=1×10°,B正确;温度不变K
不变,溶液中存在c(Ba2+)·c(C0)=K,(BaC0,),加入适量BaCl2固体,溶液中c(Ba2+)增大,c(C0)减小,-lgc(C0)增大,可使溶液由b点变到a点,C错误;当c(Ba2*)=1×1051mol·L时,d点-lgc(S0?)=y2,即c(S02)=10mol·L,c点-lgc(C0)=y1,即c(C0g)=10ml·L',两溶液中c(S02)
10c(C03)107=1012,D错误13.D【考查点】本题考查电化学
【解析】由装置连接电源可知,该装置为电解池,石墨电极上B转化为Br2,发生失电子的氧化反应,作阳极;铅电极上乙二酸转化为乙醛酸,发生得电子的还原反应,作阴极
KBr在阳极区参与循环反应,KBr不只起电解质的作用,A错误;阳极上0000的电极反应式为2Br-2e一Br2,B错误;阴极区发生反应:H0一C一C一0H+2H+2eHO-H+H,0,阳极0000区发生反应:2Br-2e—Br2、Br2+H-CC-H+20HH0一CC—H+2Br+H,0,制得2mol(阴阳两极各得到1mol)乙醛酸时,外电路中转移2mol电子,C错误;电解池中阳离子向阴极迁移,故H在外电场作用下向铅电极方向迁移,D正确
26.(14分)(1)①2AgI+Fe=2Ag+Fe2++2I(2分)AgN0,(1分)②FeL2+Cl2=L2+FeCl2(2分)L2、FeCl,(2分)I2被进一步氧化(2分】(2)2I0,+5HS0=L,+5S0+H,0+3H(2分)(3)4(1分)防止单质碘析出(2分)【考查点】本题考查无机综合
【解析】(1)①向净化除氯后含I海水中加入AgNO,发生反应:Ag+「一Agl↓,得到悬浊液,向悬浊液中加入Fe粉发生反应:2AgI+Fe一2Ag+Fe2+2I,生成的沉淀为Ag,Ag与硝酸反应生成的AgNO,可返回富集工序循环使用
②过滤后向滤液中通入Cl2,由于还原性:I「>Fe2,通入Cl2的过程中,若氧化产物只有一种,即只氧化I「,发生反应的化学方程式为FeL2+Cl2一I2+FeCl2;当反应物用量比n(Cl2)(Fel,)1.5时,发生反应:@,+2r一上+20、CL+Fe”一Cr+pe,「、e均完全被架化,放氧化产物为1:当品1.5时,过量的a,会进步氧化,发生反位:50+60一2010HC1,使单质碘的收率降低
(2)NalI0,具有氧化性,NaHS0,具有还原性,二者可发生反应:I0,+3HS0;一I厂+3S0+3H①,生成的I厂与I0;在酸性条件下发生归中反应生成12:5+I0+6H一3L2+3H,0②,由5×①+②消去中间产物I「,化简可得制备12的总反应的离子方程式
(3)KI溶液和CuS04溶液反应生成Cul沉淀和L2的离子方程式为4+2Cu2+一2Cul↓+12,故生成1molL2至少消耗4molKI:由碘微溶于水知,12在水中的溶解度较小,过量KI可使1+一I平衡正向移动,将12转化为I存在于溶液中,防止因1,析出降低高纯碘的产率
27.(15分)(1)A、C(2分》(2)Cu0+H,S0,△CS0,+H,0(2分)不产生S0,(硫酸利用率高)(1分)(3)过滤(1分)干燥(1分)除尽铁和抑制CuS0,水解(2分)破坏Fe(OH),胶体易于过滤(2分)114母卷·2021年全国甲卷·化学
安徽省宣城市2025届九年级学情调研物理试卷答案第一部分
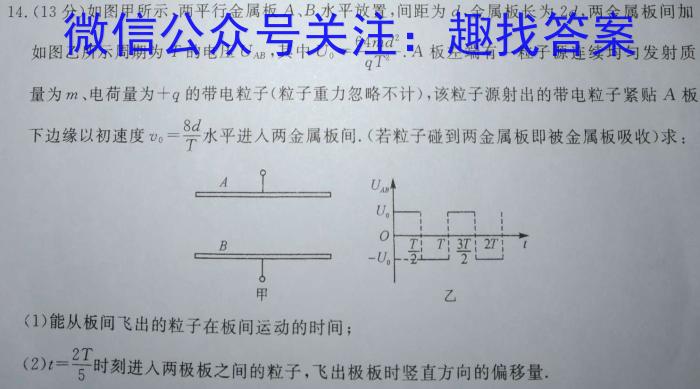
14.(13分)如图甲所示,两平行金属板A、B水平放置,间距为d,金属板长为2d,,两金属板间加如图乙所示周期为T的电压UAB,其中U0=64md^2qT^2.A板左端有一粒子源连续均匀发射质量为m、电荷量为+q的带电粒子(粒子重力忽略不计),该粒子源射出的带电粒子紧贴A板下边缘以初速度v0=8dT水平进入两金属板间,(若粒子碰到两金属板即被金属板吸收)求:(1)能从板间飞出的粒子在板间运动的时间;(2)t=2T5时刻进入两极板之间的粒子,飞出极板时竖直方向的偏移量.
安徽省宣城市2025届九年级学情调研物理试卷答案第二部分(待更新)

(1)让小球紧享因定挡板,由静止秤放,光电计时器记录小球过光电门1和光电门2所用的时间.测出两光电门间的高度差A,小球直径为d,则小球经过光电门1的速座大小v1=,小球经过光电门2的速度大小v1=。(用得的物理量符号表示)

